NETs与活化血小板相互作用增强颈内动脉闭塞卒中患者的促凝活性
...
NETs与活化血小板相互作用增强颈内动脉闭塞卒中患者的促凝活性
动脉粥样硬化血栓形成及继发性缺血性卒中一直是神经科学领域的重大临床挑战,中性粒细胞及其胞外诱捕网(NETs)与血栓炎症的相互作用逐渐成为研究焦点。2020年2月,哈尔滨医科大学第二附属医院神经外科胡韶山教授团队在 EBioMedicine(IF:10.8,中科院2区Top)在线发表了题为“Interactions between neutrophil extracellular traps and activated platelets enhance procoagulant activity in acute stroke patients with ICA occlusion”的重要研究,揭示了NETs在卒中血栓形成及高凝状态中一系列此前未被充分认识的关键机制。研究结果显示:
①在颈内动脉闭塞卒中患者的颈动脉病变部位(CLS),NETs、PLTs及PMPs显著聚集,形成促血栓形成的局部微环境。
②NETs表面暴露PS,并与PLTs相互作用。这种PS阳性的NETs为PMPs和凝血因子提供了组装平台,极大增强了凝血酶生成和纤维蛋白形成,直接驱动高凝状态。
③中性粒细胞的活化与PS暴露依赖于“两步”机制:卒中患者血浆诱导中性粒细胞预激活(第一步),随后与局部经凝血酶激活的血小板相互作用,触发PS阳性NETs的释放(第二步)。
④NETs及其相关的蛋白酶(如MMP9、NE)和组蛋白对内皮细胞具有细胞毒性,能破坏内皮屏障,并诱导内皮细胞表达TF和暴露PS,使其转化为促凝血表型,进一步放大血栓形成信号。
⑤通过药物降解NETs的DNA骨架(DNase I)或阻断其表面PS暴露(乳凝集素),以及使用西维来司他钠抑制中性粒细胞弹性蛋白酶,均可显著抑制NETs的促凝活性,并减轻内皮损伤。这为靶向NETs治疗卒中相关血栓形成提供了潜在的干预策略。
背景:中性粒细胞胞外诱捕网(NETs)在因颈内动脉(ICA)血栓栓塞闭塞导致的卒中患者中促凝活性(PCA)中的作用尚不明确。本研究旨在评估NETs在诱导卒中高凝状态中的关键作用,并阐明其在动脉粥样硬化血栓形成过程中的功能。
方法:检测55例卒中患者及35例健康对照者血浆中NETs、活化血小板(PLTs)及血小板衍生物微粒(PMPs)水平。采用免疫荧光技术分析NETs形成及血栓结构,通过流式细胞术与共聚焦显微镜检测暴露的磷脂酰丝氨酸(PS)。采用纯化凝血复合物、凝血酶及纤维蛋白形成检测法分析凝血活酶活性。
结果:颈动脉病变部位(CLS)的NETs、PLTs及PMP标志物血浆水平显著高于主动脉血。在动脉血栓及颈内动脉闭塞患者的CLS血浆中,NETs表面均呈现PS阳性。值得注意的是,CLS血浆与凝血酶激活血小板的协同作用对NETs形成及后续PS暴露至关重要。带PS的NETs为PMPs及凝血因子沉积提供了功能平台,从而促进凝血酶和纤维蛋白生成。DNase I和乳凝集素显著抑制了这些效应。此外,NETs对内皮细胞具有细胞毒性,可诱导其转化为促凝血表型。西维来司他钠、抗MMP9抗体及活化蛋白C(APC)分别以25%、39%和52%的抑制率阻断了该细胞毒性作用。
结论:NETs在卒中患者高凝状态中发挥关键作用。阻断NETs形成的策略可能为血栓栓塞干预提供潜在治疗方案。
背景研究
本研究前的证据
尽管现代药物治疗和介入治疗取得进展,动脉血栓并发症仍是导致急性缺血性卒中(AIS)最严重的临床负担之一,其潜在机制尚不明确。近期研究发现中性粒细胞能产生中性粒细胞胞外诱捕网(NETs),为揭示中性粒细胞与血栓炎症的关联提供了新途径。已有研究在AIS患者血栓或血浆中检测到NETs存在,但这些研究未解答NETs是否促进凝血及其作用机制,也未阐明NETs与PS+血小板、血小板衍生物微粒(PMPs)及内皮细胞之间的关联。
本研究的创新价值
本研究发现,在颈内动脉(ICA)闭塞过程中,于斑块破裂部位招募的中性粒细胞经血小板-中性粒细胞相互作用激活后,会释放表面装饰有功能性PS的NETs。结果还显示血小板微粒与凝血因子可附着于NETs,证明NETs结构参与卒中患者体内凝血酶和纤维蛋白的形成,从而构成动脉粥样血栓形成的组装平台。此外,NETs相关的蛋白酶和组蛋白可通过诱导内皮细胞暴露PS及表达组织因子(TF),传播并放大内皮屏障功能障碍,诱导促凝血表型。
现有证据的启示
NETs的形成在颈内动脉闭塞型缺血性卒中患者的高凝状态及急性血栓并发症中起关键作用。阻断NETs形成或局部中和其介导的磷脂暴露,可成为潜在治疗策略。此外,未来治疗方案可聚焦于联合经典抗凝药物与抗NETs策略,以进一步降低血栓风险。
rId7
动脉粥样硬化斑块破裂及继发性粥样血栓形成是急性缺血性卒中(AIS)的病理特征。约29%至56%的AIS患者在颅内大动脉闭塞后,于3个月随访时仍存在严重残疾及死亡风险。现有研究表明,AIS患者的凝血因子及标志物(D-二聚体、纤维蛋白原和微粒)水平升高。然而,动脉粥样血栓形成的精确机制,特别是关于AIS高凝状态的机制,仍未完全阐明。此外,由于对潜在病理生理机制的认识有限,目前所有抗血栓治疗均伴随不可避免的出血风险。因此,亟需开发有效治疗手段及靶点以预防或治疗AIS患者的动脉粥样血栓形成。
在众多促进血栓形成的炎症细胞和凝血介质中,越来越多的证据表明多形核中性粒细胞(PMNs)和中性粒细胞胞外诱捕网(NETs)在炎症相关血栓性疾病中发挥着关键作用。然而,中性粒细胞在脑动脉血栓形成中的作用尚未得到充分研究。近期研究发现中性粒细胞计数与卒中复发风险升高、预后不良及下游微血管血栓炎症密切相关。此外,研究证实缺血性卒中患者血栓或血浆中存在NETs,但这些研究尚未阐明NETs是否及如何促进凝血,以及其如何导致高凝状态。
现有研究表明活化血小板(PLTs)通过细胞间接触或可溶性介质对NETs形成不可或缺。反之,NETs结构中含有组织因子(TF)、von Willebrand因子(vWF)及组蛋白,为血小板黏附、活化和聚集提供支架。此外,我们先前研究发现,AIS患者血小板常处于激活状态,表现为磷脂酰丝氨酸(PS)阳性细胞数量增加及磷脂酰丝氨酸颗粒(PMPs)释放增强。然而,关于NETs、血小板和PMPs之间相互作用及其在卒中患者凝血级联激活中的作用机制仍知之甚少。组织学研究还发现,由于斑块侵蚀、破裂或斑块内出血,复杂动脉粥样硬化血栓性斑块中存在NETs。研究发现,NETs的细胞毒性可导致内皮细胞(EC)凋亡和脱落,这种现象在表层侵蚀斑块中尤为显著。然而,NETs如何引发内皮细胞活化并增强斑块促血栓形成能力仍需深入探究。
本研究通过分析主动脉或颈动脉病变部位(CLS)血样中释放NETs并暴露PS的中性粒细胞差异,评估了PLTs、PMPs与NETs间的复杂相互作用,并评估了NET-PMP复合物对颈内动脉(ICA)闭塞卒中患者促凝活性(PCA)的贡献。此外,本研究揭示了NETs通过传播与放大内皮屏障功能障碍并诱导促凝血表型的新机制。这些新发现使我们确信NETs可能在ICA闭塞患者的PCA中发挥关键作用,为预防该类卒中患者的病理性高凝状态及再闭塞提供了有前景的治疗策略。
1 .受试者特征
健康受试者与颈内动脉闭塞性卒中患者的特征汇总于表1。两组在主要的临床和实验室特征方面具有可比性。然而,卒中患者的D-二聚体、纤维蛋白原及C反应蛋白水平均高于健康对照组,提示颈内动脉闭塞性卒中患者存在高凝状态。此外,患者中性粒细胞计数亦高于健康对照组。
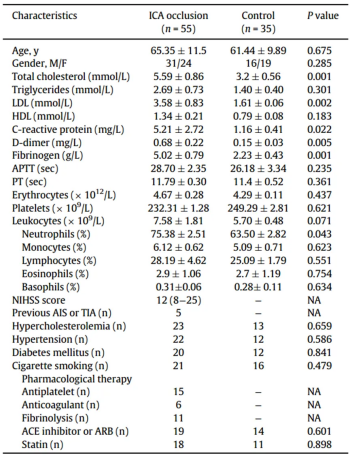
HDL,高密度脂蛋白;LDL,低密度脂蛋白;APTT,活化部分凝血活酶时间;NA,数据缺失;PT,凝血酶原时间;APTT,活化部分凝血活酶时间;ICA,颈内动脉;NIHCC,美国国立卫生研究院卒中量表;AIS,急性缺血性卒中;TIA,短暂性脑缺血发作。数据以均值±标准差表示,除非另有说明。P < 0.05视为具有统计学意义。
2 .颈内动脉闭塞性卒中患者闭塞部位NETs聚集
图1a及补充图S1展示了主动脉与闭塞部位采样示意图及支架取栓术中代表性影像。我们观察到,从ICA闭塞患者CLS附近的抽吸导管处采集的血液样本中分离出的体外中性粒细胞会释放NETs;与其他组相比,NETs释放细胞数量存在显著差异(图1b和c)。免疫荧光显微镜和蛋白质印迹分析也证实了CLS样本中NETs存在MMP-9(补充图S2)。与主动脉样本或对照组相比,CLS样本血浆中NETs特异性标志物(包括MPO-DNA、H3Cit-DNA、NE-DNA复合物及cfDNA)均呈升高趋势(图1d-g)。此外,在颈内动脉闭塞患者中,cfDNA与循环NETs-DNA复合物的水平呈显著正相关(补充图S3),表明cfDNA至少部分源自中性粒细胞。免疫荧光染色进一步证实,细胞外DNA与H3Cit及粒细胞标志物CD66b呈共定位,提示中性粒细胞和NETs存在于颈动脉血栓中。相比之下,在同源患者血液中自发形成的体外凝块中罕见中性粒细胞和NETs(图1h)。值得注意的是,颈动脉血栓所含细胞外DNA量几乎是体外凝块的4倍(图1i)。
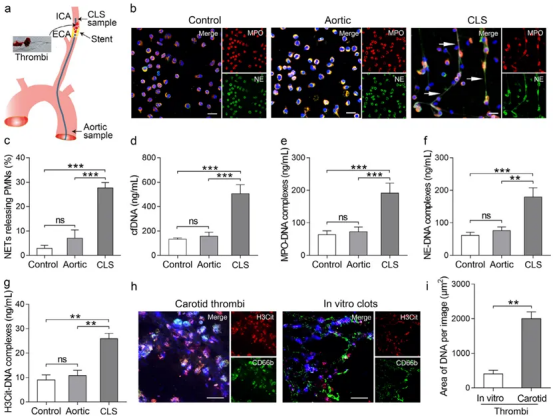
图1. CLS处NETs的聚集情况。(a)支架取栓术中主动脉与CLS取样的示意图。(b)代表性免疫荧光图像显示来自CLS、主动脉或对照样本的PMNs释放的NETs. NETs通过神经氨酸酶(NE,绿色)、髓过氧化物酶(MPO,红色)和DNA(蓝色)进行特征标记。箭头指示NETs分布。(c)选择性采血获得的分离中性粒细胞中释放NETs的细胞比例。(d-g)测定循环游离DNA(cfDNA)、H3Cit-DNA、MPO-DNA及NE-DNA复合物水平。(h) 通过粒细胞标记物CD66b(绿色)与H3Cit(红色)及DNA(蓝色)的共染色,在颈动脉血栓中可视化NETs。采用同源患者血液制备的体外凝块作为参考血栓材料。(i) 通过定制MATLAB程序分析图像,将每个像素阳性信号量化为图像中DNA面积。数据以均值±标准差表示。图(a)和(h)分别展示七次及八次独立实验中的代表性结果。统计分析采用单因素方差分析。**P < 0.01, ***P < 0.001, ns = 无统计学意义。刻度条代表50μm。对于(d)至(g)组:对照样本n=35;主动脉样本n=55;CLS样本n=55。(图例中颜色标记的具体含义请参阅本文网络版说明。)
3 .颈内动脉闭塞患者血细胞上PS暴露呈差异性分布
微粒体和血细胞表面的PS为凝血因子活化提供结合位点,是凝血级联反应的关键催化剂。乳糖粘附蛋白作为PS的特异性探针和有效阻断剂,可用于检测MPs表面的PS暴露,其检测灵敏度优于annexin V。因此我们采用乳糖粘附蛋白测定中性粒细胞和血小板的PS暴露水平。如图2a所示,对照组中性粒细胞呈现正常分叶状核形态。相反,主动脉样本中的中性粒细胞核失去分叶形态,呈现扩张状态,并出现乳酸粘蛋白的弥漫性边缘染色。在冠状动脉样本中,中性粒细胞的细胞外DNA形成网状丝状结构,并与乳酸粘蛋白同时染色。流式细胞术显示,来自颈内动脉闭塞患者的CLS样本和主动脉样本中分离的中性粒细胞,其PS暴露水平均高于健康对照组(图2b及补充图S4)。CLS样本中检测到的PS+血小板和中性粒细胞数量显著高于主动脉样本及健康对照组(图2c和d)。流式细胞分析显示,CLS来源血小板的P-选择素(CD62P,图2e)及血小板/中性粒细胞聚集物(CD41a+/CD66b+计数,图2f)水平较其他组显著升高。乳凝集素阳性血小板与PMPs、CD62P阳性血小板及血小板/中性粒细胞聚集物的平均百分比详见补充表1。如图2g所示,共聚焦显微镜图像表明对照组血小板未呈现乳凝集素染色,而颈动脉血栓样本中的血小板膜则显示强烈的乳凝集素结合。此外,经免疫荧光显微镜乳糖粘附蛋白/H3Cit双重染色观察,颈动脉血栓显示NETs和PS定位,而体外凝块中几乎未检测到PS(图2h)。
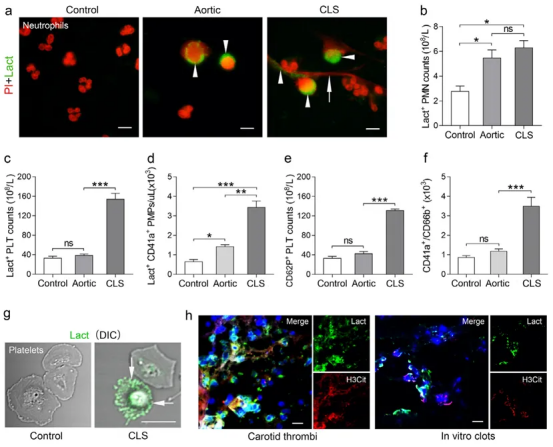
图2. PMNs和PLTs上磷脂暴露的定量分析与定位。(a)代表性免疫荧光图像显示经乳糖粘附素(绿色)和吲哚啉(红色)染色的选择性血液采样获得的多形核白细胞。对照组PMNs几乎未被乳凝集素标记。主动脉样本中,PMNs核失去分叶状形态,从破裂细胞中溢出,并呈现乳凝集素弥漫性边缘染色(箭头)。CLS样本中,PMNs胞外DNA形成网状丝状结构(箭头),同时与乳凝集素发生共染(箭头)。(b) 通过流式细胞术测定PMNs的乳糖粘蛋白结合阳性(PS+)细胞计数。同时测定乳糖粘蛋白阳性血小板(c)、乳糖粘蛋白阳性巨噬细胞(d)及CD62P阳性血小板(e)的计数。(f) 通过流式细胞术分析中性粒细胞中每10,000个CD66b+事件中CD41a+/CD66b+的数量定义血小板/中性粒细胞聚集。(g) 对对照组和CLS血样中的血小板进行乳糖粘附蛋白染色(绿色,箭头),并通过共聚焦显微镜成像。(h) 颈动脉闭塞患者血栓标本中NETs表面PS(乳糖粘蛋白,绿色)与H3Cit(红色)及DNA(蓝色)呈共定位。数据以均值±标准差表示。图示为六组(a, g)或八组(h)独立实验中的代表性结果。统计学分析采用单因素方差分析。*P < 0.05, **P < 0.01 和 ***P < 0.001, ns = 无统计学意义。图中刻度尺比例:(a)、(h)为50μm,(g)为5μm。对照组样本(b-f):n=35;主动脉样本:n=55;CLS样本:n=55。(图例中颜色标识的具体含义请参阅本文网络版说明。)
颈内动脉闭塞患者闭塞部位的局部NETs形成与PS暴露现象表明,这些结构可能是该疾病高凝状态的关键参与者。接下来,我们旨在探究颈内动脉闭塞的循环微环境是否能诱导中性粒细胞发生NETosis及PS暴露。
4 .CLS血浆诱导PS暴露但不诱导NETosis
首先,我们评估了来自颈内动脉闭塞患者的血浆对PS暴露的影响。经CLS或主动脉血浆处理的中性粒细胞,其PS暴露水平较对照组血浆处理的粒细胞显著升高(图3a和b)。其次,我们评估了不同来源血浆对NETs释放的影响。然而未检测到NETs生成显著增加(图3c和d)。进一步流式细胞术分析显示,乳凝集素和CD62P表达水平表明,CLS血浆能增强对照组血小板的活化能力,而主动脉血浆或对照血浆则无此效应(图3e,P<0.01)。我们还发现,CLS样本中CD41a+乳糖粘附蛋白+血小板的平均百分比显著高于ICA闭塞患者主动脉样本(图3f,P<0.001)。同样,与主动脉血浆和健康对照组血浆相比,对照组血小板在CLS血浆刺激后PMP水平显著升高(图3g)。
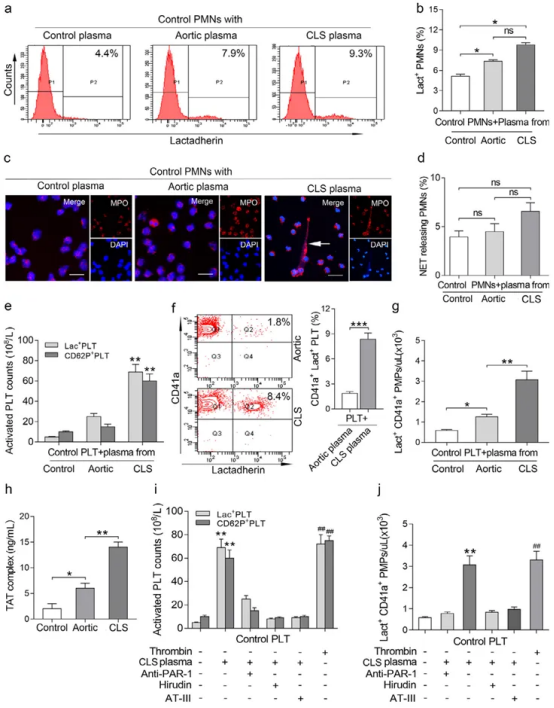
图3. 颈内动脉闭塞微环境诱导PS暴露但不诱导NETs。(a和b) 通过乳糖粘蛋白染色结合流式细胞术检测刺激后中性粒细胞的PS暴露。(c) 经CLS样本、主动脉样本或对照样本血浆处理的对照组PMN中NETs形成的代表性免疫荧光图像。NETs通过MPO(红色)和DNA(蓝色)染色标记。箭头指示NETs。展示五次独立实验的代表性图像。(d) 经选择性采血获得的血浆孵育后,对照组PMN中释放NETs的比例。(e) 经CLS、主动脉或对照血浆处理的对照血小板上乳糖粘蛋白和CD62P的流式细胞分析。(f) 密度图中激活血小板(CD41a+乳糖粘蛋白+)的比例经定量分析。(g) 经选择性采血获得血浆刺激后,对照血小板中观察到乳糖粘蛋白+前体膜颗粒水平。(h) 通过TAT复合物ELISA测定选择性采样获得的凝血酶水平。对照血小板在有或无凝血酶抑制剂(AT-III或肝素)及PAR-1抑制剂存在下接受CLS血浆处理。重组凝血酶作为阳性对照。通过流式细胞术分析检测PLTs(i)及乳凝集素阳性PMPs(j)。比例尺:50 μm。数据以均值±标准差表示。统计方法:单因素方差分析。##P < 0.01, **P < 0.01 表示与(i)和(j)中对照组及抑制剂处理组相比显著差异;*P < 0.05, ***P < 0.001;ns = 无统计学意义。图例说明:(a) (b) (d) n=17。(e) (j) n=18。(图中颜色标记的具体含义请参阅本文网络版说明。)
鉴于凝血酶可通过蛋白酶激活受体(PARs)激活血小板,我们考察了凝血酶对CLS血小板活化的影响。首先通过TAT复合物ELISA检测血浆中凝血酶水平。如图3h所示,CLS血浆中TAT复合物水平较主动脉组或对照组显著升高。此外,添加抗凝血酶III(凝血酶抑制剂)、肝素或特异性PAR-1拮抗剂后,血小板活化及PS阳性的PMPs显著减少,表明CLS血浆诱导的血小板活化具有凝血酶依赖性(图3i和j)。
5 .CLS处PLTs促成NETs生成
血小板在多种血栓性疾病中参与NETs形成。因此我们检测了颈内动脉闭塞患者CLS处血小板是否参与NETs生成。经CLS血小板处理的对照组中性粒细胞显示NETs释放显著增加,而主动脉血小板或对照组血小板处理则未促进NETs形成(图4a-c)。值得注意的是,当未添加CLS血浆时,PLTs形成的NETs表面未见磷脂A暴露(图4a)。与CLS血小板类似,体外PLTs同样能刺激对照组中性粒细胞产生无磷脂A的NETs(图4d)。此外,联合使用抗凝血酶III、蛭素或PAR-1拮抗剂可显著抑制CLS血浆激活血小板诱导的NETs生成(图4e和f,补充图S5)。
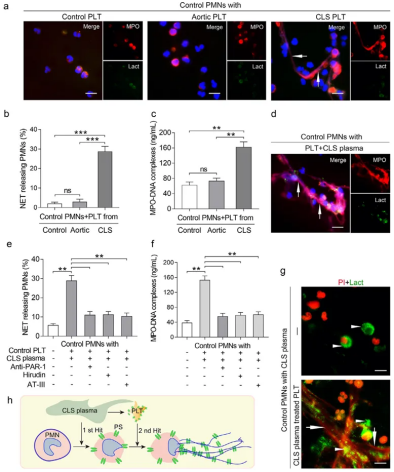
图4. 血浆与血小板在带PS的NETs形成中的作用。(a) 经选择性采血分离的血小板处理后,对照中性粒细胞(PMNs)产生的NETs。通过免疫荧光显微镜观察到乳凝集素(绿色)、髓过氧化物酶(MPO,红色箭头)和DAPI(蓝色)的存在。展示六次独立实验的代表性图像。(b) 经选择性采血分离的血小板处理后,NETs释放性PMN比例的定量分析;(c) 上清液中MPO-DNA复合物浓度测定。PMN在有/无AT-III、肝素或PAR-1拮抗剂存在下,与未刺激或经CLS血浆刺激的血小板共同培养。(d) 代表性免疫荧光染色图像:PS暴露(乳凝集素,绿色)与NETs形成(MPO,红色,箭头标记)。(e) NETs释放中性粒细胞百分比及(f) MPO-DNA复合物水平评估。(g) 对照组PMNs经CLS血浆刺激及预处理CLS血浆的对照组血小板后产生的PS阳性NETs。PMNs免疫荧光代表性图像经乳凝集素(绿色)和PI(红色)染色。细胞外DNA扩散至细胞外空间(箭头),并与乳凝集素呈共定位染色(箭头)。(h) 抗原呈递分子结合性NETs形成的“两步”过程模型。数据以均值±标准差表示。图(d)展示六次独立实验之一,图(g)展示五次独立实验之一。统计方法:单因素方差分析。比例尺:20 μm。**P < 0.01,***P < 0.001,ns = 无统计学意义。图(b)(c)(e)(f)样本量n=15。(本图例中颜色标记的具体含义,请参阅本文网络版说明。)
我们通过“双重刺激”实验流程进一步探究血小板与血浆在PS阳性NETs形成中的协同作用。首先,在与颈内动脉闭塞患者的CLS血浆孵育后,测定中性粒细胞的PS暴露水平。随后,如前所述,向这些PS+中性粒细胞中添加PLTs(CLS血小板或体外PLTs)以刺激NETs生成(图4g和h)。
6 .CLS处的NETs-PMP复合物促进凝血酶与纤维蛋白形成
为阐明PS阳性NETs在ICA闭塞患者促凝活性PCA中的功能,我们探究了PMPs能否体外结合NETs从而促进患者PCA增强。结果表明PMPs可附着于NETs,证实NETs为PMPs提供了组装平台(图5a)。通过APC切割组蛋白、DNase I降解DNA支架或乳凝集素阻断PS,分别使PMP黏附程度降低64.3%、56.5%和47.5%(图5b,P<0.01)。随后我们设计实验量化内源性凝血因子与NETs的结合。检测到凝血因子(凝血酶原、纤维蛋白原和X因子)与NETs结构的结合(图5c),表明这些结构可作为凝血酶原酶复合物的组装位点。我们评估了构成NETs的DNA、组蛋白和PS在促进凝血因子结合中的作用。类似地,经DNase I、活化蛋白C(APC)和乳凝集素处理后,凝血因子黏附程度显著降低(图5d,P<0.01)。
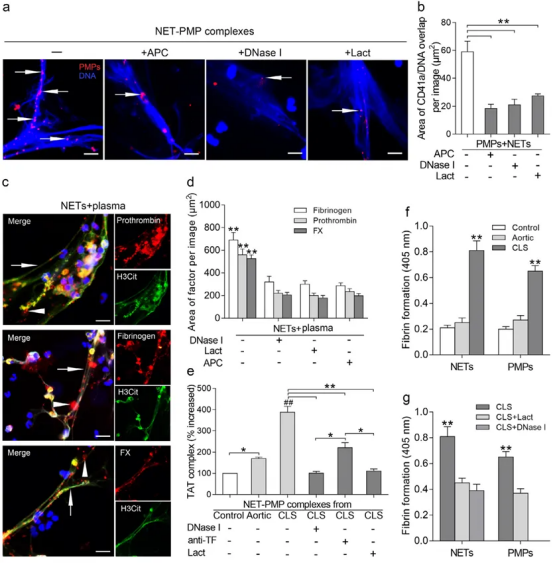
图5. NETs-PMP复合物的形成及其在PCA中的作用。(a) 代表性免疫荧光图像显示PMPs附着于NETs。PMPs用CD41a标记(红色,箭头),细胞外DNA用DAPI染色(蓝色)。经APC、DNase I及乳凝集素处理后,PMPs粘附被抑制。(b) 通过定制MATLAB程序分析免疫荧光图像,将每个像素阳性信号量化为图像中CD41a与DNA信号的叠加面积。(c) 代表性免疫荧光图像显示凝血因子:凝血酶原、纤维蛋白原和X因子(红色,箭头)结合至NETs(H3Cit,箭头)。(d) 抑制实验中,中性粒细胞预先用乳凝集素、DNase I或APC处理,随后量化结合NETs的凝血因子面积。(e) 采用TAT复合物ELISA分析凝血酶水平。对照血浆与选择性采血样本中分离的NETs-PMP复合物孵育后测定凝血酶浓度。样本经DNase I、抗TF抗体或乳凝集素预处理以抑制凝血酶生成。(f) 采用浊度法检测NETs与PMP支持纤维蛋白形成的能力。于405 nm波长监测纤维蛋白聚合。(g) 通过CLS样本验证乳凝集素或DNase I对纤维蛋白形成的抑制作用。数据以均值±标准差表示。图(a)展示六组独立实验之一,图(c)展示四组独立实验之一。统计分析采用单因素方差分析。比例尺:50μm。**P < 0.01 表示与(f)中对照组或主动脉组相比显著差异。**P < 0.01 表示与(g)中DNase I或乳凝集素处理组相比显著差异。*P < 0.05, **P < 0.01。**P < 0.01 较DNase、乳凝集素或APC处理组(d);##P < 0.01 较对照组或主动脉组(e)。(d-g组n=18)。(图例中颜色标记的解释请参阅本文网络版说明。)
由于抑制剂能降低NETs-PMPs或NETs-凝血因子结合能力,其亦可减轻NETs的促血栓表型。在研究NETs-PMP复合物的PCA时,我们发现与其他组别分离的NETs-PMP复合物相比,经CLS样本获得的NETs-PMP复合物与血浆孵育后,TAT水平显著升高(图5e)。DNase I降解染色质支架或乳凝集素阻断PS后,凝血酶生成量分别降低72%和65%。添加中和性抗TF抗体作用有限(图5e)。随后我们评估了NETs与PMP促进纤维蛋白形成的活性。CLS样本中的NETs和PMPs诱导的纤维蛋白生成量显著高于其他组别(图5f,P<0.01)。乳凝集素或DNase I可有效抑制纤维蛋白形成(图5g,P<0.01),表明带PS的NETs与PS+ PMPs共同参与了ICA闭塞相关的高凝状态。
7 .NETs相关蛋白酶与组蛋白诱导内皮细胞活化
NETs的形成可激活内皮细胞,甚至引发其死亡,且NETs与人类动脉粥样硬化斑块中的凋亡内皮细胞相关。因此我们探究从颈内动脉闭塞患者血栓溶解液中分离的NETs是否能激活内皮细胞。为验证该假说,我们评估了不同浓度NETs作用不同时间后对人脐静脉内皮细胞(HUVECs)中ICAM-1和VCAM-1的表达影响。在高浓度NETs(0.5 mg DNA/mL)作用下,12小时后VCAM-1和ICAM-1表达水平均显著上升,并在24小时达到峰值(图6a 鉴于内皮细胞黏附与内皮完整性依赖于连接蛋白,我们进一步通过共聚焦显微镜、流式细胞术和蛋白质印迹技术评估了细胞间连接蛋白CD31和VE-钙粘蛋白的表达。结果显示,与对照组相比,NETs处理的内皮细胞中CD31和VE-钙粘蛋白表达水平均显著降低。CD31和VE-cadherin分别是MMP9和NE的底物。我们随后评估了抑制MMP9或NE活性是否能防止这些连接蛋白的减少。如图6e-h所示,用抗MMP9抗体或NE选择性抑制剂西维来司他钠预处理NETs后,分别减轻了NETs诱导的CD31或VE-钙粘蛋白表达缺失。为进一步验证西维来司他钠和抗MMP9抗体的特异性,我们进行了交叉实验。如补充图S6所示,用西维来司他钠预处理NETs并未消除NETs诱导的CD31表达丢失。同样,用抗MMP9抗体抑制MMP9也未显著改变内皮细胞的VE-钙粘蛋白表达水平。
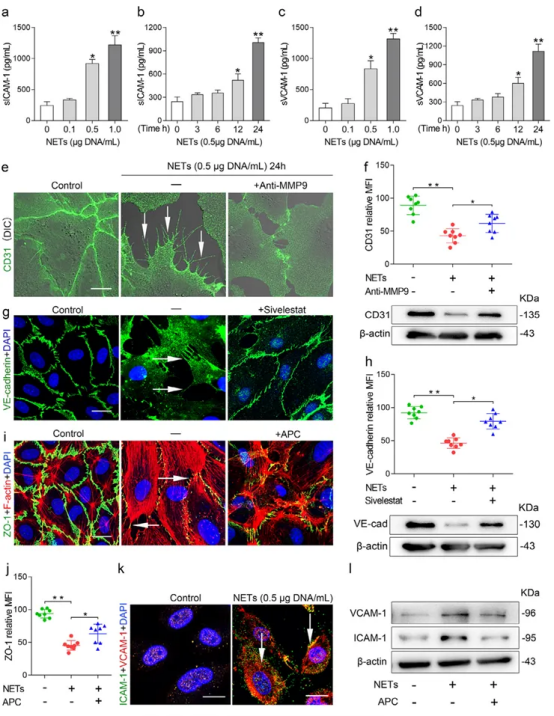
图6. NETs对人脐静脉内皮细胞(HUVECs)的细胞毒性作用。(a-d) HUVECs与不同浓度的NETs或NETs(0.5 mg DNA/mL)共同培养指定时间。通过ELISA检测ICAM-1和VCAM-1表达水平。免疫荧光成像(e, g, i)及流式细胞术(f, h)结果显示,经NETs(0.5 mg DNA/mL)刺激24小时后,HUVECs上CD31、VE-钙粘蛋白 及ZO-1的表达均呈现下降趋势(通过免疫荧光成像[e,g,i]、流式细胞术[f,h上图及j,表达以平均荧光强度[MFI]表示]及蛋白质印迹分析[f,h下图]验证)。共聚焦显微镜图像清晰显示细胞边缘收缩及丝状伪足伸展(箭头),表明内皮细胞间连接受损。NETs诱导F-肌动蛋白束向中心聚集,提示肌动蛋白应力纤维形成。抑制实验中,分别在有/无抗MMP9抗体、西维来司他钠或APC存在下,将HUVECs与NETs共同孵育。(k) 代表性共聚焦显微镜观察显示,ICAM-1(红色)和VCAM-1(绿色)分布于HUVECs表面(箭头)。(l) ICAM-1和VCAM-1蛋白表达经蛋白质印迹分析检测。数据以均值±标准差表示。展示八次(e, g, i)或六次(k)独立实验中的代表性结果。统计学分析采用单因素方差分析或学生t检验。*P < 0.05, **P < 0.01。比例尺:5 μm。*P < 0.05, **P < 0.01 表示相较于(a)组对照组显著差异。其中(a)组样本量n=10,(f)(h)(j)组样本量n=8。(图例中颜色标记的具体含义请参阅本文网络版说明。)
为进一步探究组蛋白的影响,我们还考察了其对细胞间连接及内皮细胞肌动蛋白细胞骨架的作用。与对照组相比,NETs刺激HUVECs后,细胞间边界处的紧密连接蛋白ZO-1迅速变薄,且F-肌动蛋白应力纤维数量增加。用APC预处理NETs可降低其介导的细胞毒性(图6i、j)。与未刺激对照组相比,经NETs处理的细胞表现出更高的VCAM-1和ICAM-1表达,而添加APC可消除此效应(图6k和l)。这些结果表明,NETs相关蛋白酶和组蛋白的存在破坏了内皮单层完整性,并引发内皮功能障碍。
8 .NETs使HUVECs转化为促凝血表型
为深入解析NETs处理后内皮细胞的促血栓形成特性,我们检测了TF和PS在内皮细胞上的表达。免疫荧光染色显示:HUVECs从细胞间边界收缩并形成丝状伪足,TF呈点状分布于细胞表面及伪足区域。经乳糖粘蛋白染色后,HUVECs呈现不规则形态并形成强绿色荧光伪足,表明存在PS暴露(图7a)。TF的mRNA表达在12小时后快速上升,于24小时达峰值。经西维来司他钠、抗MMP9抗体及APC预处理后,NETs诱导的TF表达完全被抑制(图7b)。流式细胞术检测显示,HUVECs在NETs存在下培养时,其PS暴露呈时间依赖性增加,12小时后快速上升并在24小时达到峰值(图7c)。西维来司他钠抑制HUVECs外露PS达25%,抗MMP9抗体抑制39%,APC抑制52%(图7c)。
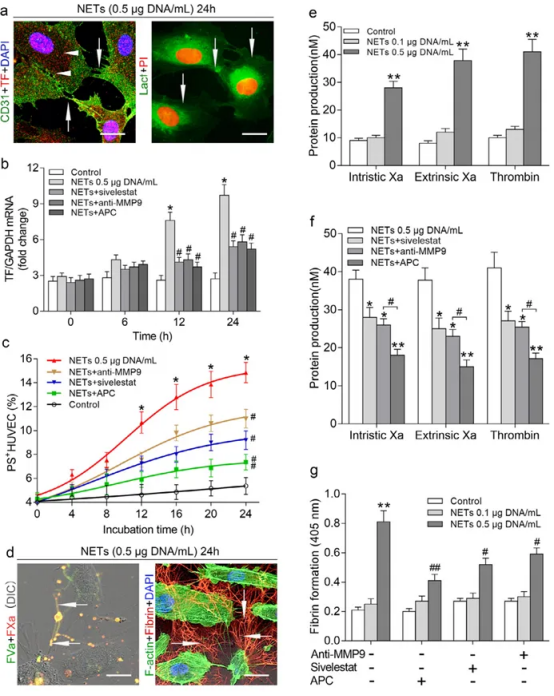
图7. NETs增强HUVECs的促血栓形成能力。(a) 典型共聚焦显微镜图像显示,HUVECs经NETs(0.5 mg DNA/mL)处理24小时后,细胞边缘收缩,丝状伪足伸展(箭头),且TF(红色)呈点状分布于HUVECs表面及丝状伪足上(箭头)。HUVECs经乳腺粘附蛋白(绿色)和PI(红色)共孵育后,呈现不规则形态并形成具强绿色荧光的伪足(箭头)。NETs(0.5 mg DNA/mL)孵育条件下HUVECs表面TF(b)和PS(c)暴露动力学变化(抑制剂存在时)。(d) 在HUVECs收缩边缘附近的丝状伪足(箭头)上观察到FVa和FXa共定位(黄色)。经NETs预处理并用健康血浆孵育的HUVECs显示显著的纤维蛋白束形成,这些纤维蛋白束沿丝状伪足(箭头)呈放射状排列,形成纤维蛋白网络。(e) 测定不同浓度NETs处理后HUVECs产生的内源性Xa、外源性Xa及凝血酶。(f) 采用西维来司他钠、抗MMP9抗体或APC抑制剂处理HUVECs前降解NETs相关弹性蛋白酶或组蛋白,进行蛋白质生成抑制实验。(g) 测定经不同浓度NETs刺激24小时的HUVECs在西维来司他钠、抗MMP9抗体或APC存在下的纤维蛋白形成情况。数据以均值±标准差表示。比例尺:5 μm。展示六组独立实验(a和d)中的一组。统计分析采用单因素方差分析或学生t检验。*P < 0.05 与对照组比较;#P < 0.05 与 NETs(0.5 mg DNA/mL)组比较(b)*P < 0.001 与对照组比较;#P < 0.05, ##P < 0.01 与 NETs 组比较(c)。**P < 0.01 与对照组或NETs组(0.1 mg DNA/mL)比较(e)和(g)。*P < 0.05,**P < 0.01 与NETs组比较(f)。#P < 0.05, ##P < 0.01 较 (g) 中西维来司他钠 (-) 抗MMP9抗体 (-) APC (-) 组。对于 (b) (c) (e) (f) (g) n = 8。(本图例中颜色标记的解释请参阅本文网络版。)
随后我们验证了TF和PS表达是否促进凝血酶原激活酶和凝血酶原酶活性的增强。共聚焦显微镜显示,经NETs处理的HUVECs上存在FVa与FXa的共定位,表明这些细胞通过表达PS和TF为凝血因子提供了大量结合平台。FVa和FXa优先结合于弯曲度高的丝状伪足和细胞边缘(图7d)。此外,当HUVECs暴露于NETs时,沿其丝状伪足形成呈放射状分布的大型纤维蛋白束(图7d)。这些结果表明,仅在高浓度NETs孵育的HUVECs中观察到FXa复合物和凝血酶表达增加(图7e,P < 0.01)。在西维列司他、抗MMP9抗体或APC存在下,FXa复合物和凝血酶的生成均减少(图7f)。其中APC相较于西维列司他和抗MMP9抗体具有显著更强的抑制效果(图7f,P<0.05)。纤维蛋白生成实验进一步证实,高浓度NETs处理组诱发的纤维蛋白形成量显著高于另两组(图7f)。西维来司他钠、抗MMP9抗体及APC均能有效抑制纤维蛋白形成(图7g)。
综上所述,本研究结果揭示了三个关键机制:首先,基于不同部位采集的血液样本,我们证实了PS阳性的NETs、PLTs及PMPs在颈动脉血栓形成部位的局部聚集。此外,PS阳性NETs的生成遵循两步程序,既需要来自颈内动脉闭塞患者的血浆,也需要主要存在于循环系统中的PLTs。其次,PMPs可通过组蛋白-PS相互作用与NETs结合;NETs-PMP复合物的聚集为凝血因子沉积提供了适宜平台,在血栓形成过程中发挥关键作用。第三,NETs相关蛋白酶与组蛋白对内皮细胞产生强效细胞毒性作用,并通过诱导PS暴露和TF表达增强内皮细胞促血栓性。
已有研究报道严重动脉粥样硬化及急性缺血性卒中患者全身血液中NETs标志物升高。本研究首次揭示:颈动脉闭塞期间聚集于闭塞血栓的中性粒细胞被激活并释放NETs,这些NETs表面装饰着暴露的PS。此外,本研究与近期缺血性卒中血栓研究结果一致,证实了颈动脉血栓中存在NETs成分,并进一步证明血栓中存在中性粒细胞及带PS的NETs。PS+的囊泡和血细胞作为凝血级联反应中凝血酶原酶复合物和凝血酶原酶复合物的必要底物,从而催化凝血酶生成和纤维蛋白形成。我们先前已证实,卒中时中性粒细胞暴露的PS显著促进了FXa复合物生成和凝血酶形成。本研究突破既往成果,首次揭示中性粒细胞胞外DNA释放与NETosis诱导的PS暴露,与纤维蛋白沉积增加及凝血酶原酶复合物形成存在关联。具有功能性PS的NETs可诱导凝血酶生成和血小板活化,从而增加动脉粥样血栓形成风险。
本研究证实,颈内动脉闭塞患者的循环微环境可促进中性粒细胞PS暴露。此外,通过体外培养中性粒细胞与ICA闭塞患者脑脊液及主动脉样本血浆,检测到PS表达上调。我们推测中性粒细胞PS暴露增加部分源于卒中后巨噬细胞产生的血浆促炎细胞因子(包括IL-1β和TNF-α)。在缺血性血管病变部位,局部中性粒细胞-血小板相互作用很可能成为NETs形成的关键因素。本研究观察到,来自罪犯颈动脉的血样中PLTs水平升高且血小板-中性粒细胞复合体数量增多。此外,与先前报告一致,CLS来源血浆诱导的血小板活化具有凝血酶依赖性。因此,我们提出动脉粥样硬化闭塞性颈内动脉病变中PS阳性NETs的“两步”发病机制模型:血浆炎症刺激增强中性粒细胞PS暴露;同时中性粒细胞与PLTs相互作用,在病变局部微环境中诱导PS阳性NETs释放。鉴于部分研究者已证实NETs通过促凝血介质(包括组织因子、第XII因子、微粒、von Willebrand因子及纤维蛋白原)参与血栓形成,我们需通过更多实验揭示这些分子与NETs支架上的磷脂的潜在相互作用。
研究发现,PMP与凝血因子附着于NETs可诱导凝血酶生成、纤维蛋白沉积及血栓形成,进而阻塞微血管,导致灌注减少和微环境改变。先前研究揭示,癌细胞来源的微粒与NETs结合,在DVT模型早期即参与血栓形成并发挥关键作用。这些研究表明NETs可招募微粒至血栓形成部位。事实上,PMPs在血液循环中最为丰富,约占所有循环微粒的70%至90%。本研究发现,颈内动脉闭塞患者的血样中PMP水平显著升高。此外,NETs为PS+ PMP提供了黏附支架,表明NETs-PMP复合物的形成可作为凝血酶原酶复合物的组装位点,促进凝血酶生成。这些结果与现有研究一致,即NMPs在体外对NETs具有高亲和力结合。值得注意的是,与乳凝集素共孵育可消除PMPs对NETs的附着,表明PMPs表面的PS介导了NETs-PMP粘附。鉴于PS可与组蛋白结合,我们推测NETs来源的组蛋白可作为PMP表达的PS配体。实验证实,APC降解组蛋白后,PMP与NETs的结合力降低64.3%。此外,NETs还含其他蛋白质,可能促进PMP-NETs相互作用或加剧内皮损伤。
近期研究表明,在DVT和AIS等多种炎症及血栓性疾病中,纤维蛋白原、细胞外DNA和vWF会在血栓内部形成共定位网络。本研究证实,颈动脉血栓中存在表面修饰有PS的NETs,并明确揭示PS阳性NETs支持凝血因子在细胞外染色质及暴露PS周围沉积。近期研究证实了这些发现。因此,NETs形成与PS暴露在动脉粥样血栓形成中发挥关键作用。本研究揭示NETs结构可能作为凝血酶原、纤维蛋白原和X因子组装的支架,为通过靶向抑制NETs和/或PS以减轻动脉粥样血栓形成提供了合理方案。值得关注的是,我们还直接证实颈内动脉闭塞患者中,围绕细胞外染色质复合体的NETs-PMP复合物可诱导凝血酶生成与纤维蛋白形成。该凝血酶原PCA可通过DNase I和/或乳凝集素抑制,而抗凝血酶原抗体中和作用效果甚微。一种合理解释是:血浆中暴露的凝血酶原常处于加密状态,其可测PCA水平极低或不可测。
在动脉粥样硬化或血栓形成发生前,血管内皮会经历促炎性改变,如异常激活或凋亡,导致血管完整性丧失。中性粒细胞及其释放的NETs是内皮损伤的早期应答者,并改变内皮细胞的抗凝功能。近期研究表明,中性粒细胞与NETs共同促进局部动脉内皮细胞活化,触发纤维蛋白原激活物活性与凝血酶生成,进而促进血栓形成。然而其具体机制尚未完全阐明。本研究发现,颈内动脉闭塞患者斑块基质中的NETs可通过诱导内皮细胞活化及增强黏附性造成内皮损伤,进而促进更多中性粒细胞聚集至斑块部位。此外,我们证实NETs可诱导HUVECs表达PS和TF,使其呈现促凝血表型。促凝血内皮细胞能为凝血因子提供大量结合位点,这可能通过PS和TF的表达实现。先前研究已证实凋亡内皮细胞具有类似的促凝活性,与本研究结果一致。
NETs相关的蛋白酶(包括MMP9和NE)在清除血管内皮细胞附着的ECM过程中发挥关键作用。该基质的破坏亦可能促进内皮细胞活化或凋亡。本研究发现,抑制NE和MMP9的活性可分别防止NETs诱导的VE-钙粘蛋白和CD31表达丢失。这些研究得到现有文献支持。然而,NETs相关蛋白酶是否影响凋亡内皮细胞的作用仍存争议。Pieterse等通过Annexin V检测发现,内皮细胞间连接的丧失并非NETs介导的内皮细胞凋亡所致,这与其他研究结果不一致。此外,近期研究证实NETs相关组蛋白可加速内皮细胞间连接丧失并诱导细胞凋亡或死亡,而APC能裂解并解毒细胞外组蛋白,这与本研究结果一致。我们的结果还表明,西维来司他钠、抗MMP9抗体和APC可抑制NETs的细胞毒性效应,从而保护内皮细胞并降低PCA,这表明它们在预防动脉粥样硬化血栓并发症中具有关键作用。
综上所述,本研究阐明了颈内动脉闭塞型急性缺血性卒中患者高凝状态及急性血栓并发症的新机制。尽管患者接受了及时的双联抗血小板治疗,其PCA仍显著增强。因此仅靠抗血小板治疗不足以完全预防血栓形成。未来治疗策略可聚焦于联合抗血小板药物与针对NETs的靶向治疗,既能进一步降低血栓风险,又可减少抗血小板药物用量并降低出血并发症发生率。
参考文献:
Zhou P, Li T, Jin J, Liu Y, Li B, Sun Q, Tian J, Zhao H, Liu Z, Ma S, Zhang S, Novakovic VA, Shi J, Hu S. Interactions between neutrophil extracellular traps and activated platelets enhance procoagulant activity in acute stroke patients with ICA occlusion. EBioMedicine. 2020 Mar;53:102671. doi: 10.1016/j.ebiom.2020.102671. Epub 2020 Feb 27. PMID: 32114386; PMCID: PMC7047181.
本文转载自独立学术期刊,仅供专业人士学术参考,不可作为诊疗依据,任何用药请严格遵循药品说明书.
推荐阅读:

